Spécialité : pathologies circonstancielles / pédiatrie /
Points importants
- Coup de chaleur d’exercice = Hyperthermie maligne d’effort = Heatstroke
- Définition : Effort prolongé + T° > 40°C + Signes neurologiques
- Complications :
- séquelles neurologiques graves
- état de choc multifactoriel
- rhabdomyolyse
- insuffisance hépatorénale
- CIVD
- défaillance multi viscérale
- Décès en l’absence de traitement précoce
- Traitement = refroidissement externe actif + remplissage vasculaire
- Refroidissement par pulvérisation d’eau tiède + évaporation par ventilateur + glace
- Immersion en eau glacée seulement si sujet jeune, sain, sportif entraîné, sans trouble de conscience et compliant
- Aucun intérêt du dantrolène et des antipyrétiques en 1ère intention
- Principaux facteurs de mauvais pronostic :
- retard du traitement
- sous-estimation de la gravité
- Objectif : traiter tôt et efficacement d’emblée +++
- Bilan étiologique chez le sujet et sa famille (implications génétiques)
Présentation clinique / CIMU
CONTEXTE
Terrain
- Sujet jeune, sportif et entraîné le plus souvent
- Sujet militaire avec fortes contraintes physiques (commandos, forces spéciales, légionnaire, marche forcée, course prolongée avec charge)
- Parfois « ancien sportif » reprenant brutalement une pratique d’endurance pour laquelle il est insuffisamment entraîné
Antécédents
- Sujet sain et sans ATCD le plus souvent
- Rarement notion d’ATCD du même type dans la famille ou chez le sujet lui-même
Facteurs de risque et comorbidités
- Fièvre pré-existante (état fébrile infectieux, fièvre inflammatoire, etc.)
- Déshydratation préalable (diarrhée profuses, vomissements, etc.)
- ATCD personnels ou familiaux de coup de chaleur d’exercice : participation génétique très probable (implication des HSP : Heat Stroke Proteins)
- Pas de lien démontré avec les ATCD d’hyperthermie maligne per-anesthésique
- Toxicomanie par substances adrénergiques ou autres, type cocaïne, ecstasy
- Obésité
- Hyperthyroïdie
- Insuffisance rénale chronique
- Insuffisance surrénalienne chronique
- Epilepsie
- Mucoviscidose
- Dermatoses exfoliantes
Facteurs favorisants
- Manque d’entraînement pour des efforts intenses et prolongés
- Manque d’acclimatation avant un effort en région chaude ± humide
- Absence d’hydratation suffisante et de protection thermique (casquette, brumisation…) avant et surtout pendant l’effort
- Privation de sommeil (décalage horaire lors d’épreuves à l’étranger)
- Consommation récente d’alcool ou de drogues (ecstasy, cocaïne +++)
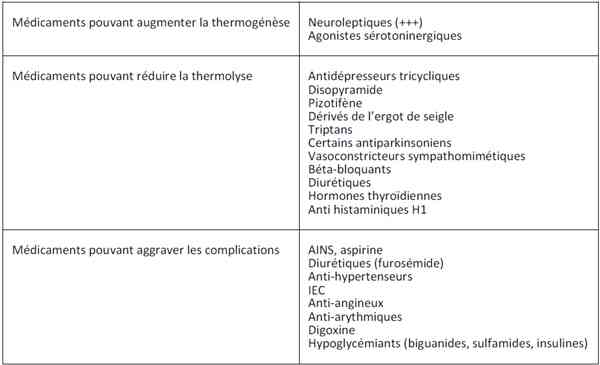
Facteurs iatrogènes
_263
- Coup de chaleur d’exercice : facteurs iatrogènes Circonstances de survenue
- Contexte de compétition dans la pratique d’un sport avec efforts longs et soutenus (marathon, triathlon, enduro)
- Ambiance le plus souvent chaude et humide, mais pas nécessairement (accident pouvant tout à fait survenir en climat tempéré)
- Situation de dépassement volontaire de ses propres limites en raison de l’objectif (compétition sportive, épreuve sportive dans le contexte d’un concours ou d’un recrutement…).
- Prodromes :
- baisse de performance en cours d’épreuve
- sensations de crampes, de chaleur intense, soif +++
- Epuisement musculaire et physique global contraignant à l’abandon
- Règle d’or : tout symptôme neurologique peut se rencontrer au cours d’un coup de chaleur d’exercice +++
- Troubles sensoriels : hallucinations et troubles visuels divers, acouphènes, bourdonnement d’oreille
- Troubles du comportement, allant parfois jusqu’à une conduite totalement inadaptée de maintien de l’effort
- Vertiges, obnubilation, syndrome confusionnel
- Convulsions, voire état de mal épileptique
- Signes neurologiques focalisés possibles : troubles de la sensibilité, déficit moteur
- Troubles de la conscience pouvant aller jusqu’au coma
- Température corporelle > 39°5 – 40°C
- Signes majeurs de déshydratation :
- extracellulaire (sécheresse des muqueuses, yeux cernées, pli cutané…)
- et intracellulaire (soif intense)
- Initialement peau chaude et humide (tant que les capacités de sudation sont maintenues)
- Classiquement peau sèche et chaude au contact (signe tardif et de gravité)
- Tout est possible !
- Etat de choc (PA moyenne < 90 mmHg, tachycardie, oligo-anurie)
- Tachypnée
- Hyperventilation (compensation de l’acidose lactique)
- Convulsion, coma
- Hémorragies extériorisées (CIVD)
- Troubles du rythme cardiaque graves secondaires à l’hyperkaliémie (TV, FV…)
- L’hypoglycémie d’effort est un diagnostic différentiel à évoquer systématiquement +++
- Recherche de SCA, de troubles du rythme, de signes évocateurs d’une hyperkaliémie menaçante
- Tri 1 à 3 selon niveau de gravité
- Syndrome d’hémoconcentration (élévation de l’hématocrite, fausse polyglobulie)
- Sepsis sévère (hyperleucocytose)
- Syndrome d’hémoconcentration (hyperprotidémie, hypernatrémie)
- Elévation de la créatininémie (insuffisance rénale aiguë multifactorielle : état de choc, rhabdomyolyse…)
- Hyperkaliémie (insuffisance rénale, rhabdomyolyse d’effort)
- Elévation des lactates (acidose lactique par effort anaérobie + état de choc et souffrances tissulaires diffuses), signe de gravité majeure
- Acidose métabolique lactique ± compensée
- TP, TCK, Facteur V, plaquettes, fibrinogène (coagulopathie de consommation)
- CPK totales, aldolase, myoglobine (rhabdomyolyse constante)
- Insuffisance coronarienne aiguë secondaire au choc (élévation de la troponine Ic, myoglobine, CPK totales)
- Hépatite aiguë cytolytique liée à l’état de choc (élévation des transaminases souvent > à 4 fois la normale)
- Pancréatite aiguë d’effort (élévation de la lipasémie et de l’amylasémie)
- VS, CRP, Procalcitonine (marqueurs pronostiques et évolutifs du sepsis)
- Prélèvements bactériologiques : 3 hémocultures aérobies + anaérobies, ECBU, ponction lombaire au moindre doute d’infection neuro-méningée
- Frottis goutte épaisse à la moindre suspicion de neuro-paludisme (sujets militaires ou provenant de l’étranger notamment)
- Alcoolémie
- Recherches d’amphétamines, cocaïne
- Recherche de médicaments potentiellement favorisants selon le contexte :
- antidépresseurs tricycliques, etc.
- Radiographie du thorax (bilan infectieux : pneumopathie ?)
- TDM ou IRM cérébrale en cas de coma, de signes de focalisation
- TDM abdominale si tableau péritonéal, etc.
Diagnostic différentiel De l’hyperthermie- Coup de chaleur d’exposition, sans effort (canicule)
- Fièvre d’origine infectieuse : choc septique, purpura fulminans
- Fièvre inflammatoire
- Hyperthermie iatrogène (syndrome malin des neuroleptiques, etc.)
- Intoxication aiguë à la cocaïne, ecstasy, amphétamines, etc.
- Insuffisance surrénalienne aiguë
- Phéochromocytome
- Crise aiguë thyréotoxique (mais fièvre rarement aussi élevée)
- Infections neuro-méningées, neuro-paludisme
- Hypoglycémie d’effort +++
- Hémorragie méningée en cours d’effort
- AVC
- Crise convulsive hyperthermique en contexte infectieux
- Syndrome confusionnel en contexte infectieux
- Delirium tremens
- Refroidissement :
- en préhospitalier : début du refroidissement et protection thermique :
- arrêt de l’effort physique en cours et repos total (allongé)
- placer le sujet dans un endroit sec, frais et à l’ombre
- déshabillage
- classiquement, immersion en eau très froide (1 à 2°C) dès que possible (technique actuellement controversée car risquée et sans bénéfice comparativement aux techniques moins agressives)
- l’immersion en eau « tempérée » environ 5° à 10°C sous la température corporelle est suffisante dans un premier temps
- à défaut d’immersion, asperger longuement le corps nu avec de l’eau tiède (15 à 20°C) tout en provoquant un courant de convection d’air : idéalement ventilateur, à défaut éventails de fortune
- aux urgences : refroidissement avec objectif de retour rapide à une température corporelle < 39°C : refroidissement externe +++
 _264
_264- Refroidissement externe
- Refroidissement externe
- technique simple, rapide à mettre en oeuvre et utilisable chez le patient perfusé, monitoré, voire intubé
- tunnel réfrigérant associant un courant d’air provoqué par un ventilateur au pied du lit propulsant l’air sous un tunnel composé de draps et d’arceaux de lits orthopédiques
- air refroidi par un bac de glace pilée devant le ventilateur
- peau régulièrement mouillée par brumisation d’eau fraîche ou apposition de linges humides
- pose de pains de glaces (interposer un linge humide) au niveau des plis inguinaux et aisselles
- immersion envisageable seulement si l’état de conscience et la mise en condition du patient le permettent
- nombreuses techniques de refroidissement internes décrites
- en préhospitalier : début du refroidissement et protection thermique :
- Réanimation symptomatique type ABCDE :
- A+B/Airway + Breathing :
- contrôle de la liberté des VAS
- oxygénothérapie au masque haute concentration à débit suffisant pour obtenir une SpO2 > 95 %
- si coma, induction à séquence rapide et ventilation mécanique
- C / Circulation : Stabilisation hémodynamique :
- poser 2 voies veineuses de gros calibre
- remplissage vasculaire de 1 à 2 L la 1ère heure, à adapter selon la réponse hémodynamique (objectif de normalisation rapide de la PA)
- soluté : NaCl 0,9% en 1ère intention, si possible à 15 – 20°C
- si collapsus sévère d’emblée ou correction insuffisante avec les cristalloïdes, recours aux solutés macromoléculaires (HEA) à haut débit dépasser 1500 mL
- recours aux médicaments vasopresseurs uniquement en cas d’échec d’une expansion volémique bien conduite : noradrénaline IVSE en débutant à 0,1 – 0,2 µg/kg/min puis adapter par paliers de 0,1 µg/kg/min
- D / Disabilities and Drugs : autres médicaments :
- dantrolène : pas d’indication démontrée en 1ère intention (mécanisme différent de l’hyperthermie maligne per-anesthésique). Utilisable uniquement en cas d’hyperthermie maligne réfractaire au refroidissement et support hémodynamique bien conduits. Dose initiale de 2,5 mg/kg IVL (en 5 min) puis compléter à 5 mg/kg IVL et poursuivre en cas d’efficacité par paliers de 1 mg/kg en IVL sans dépasser une dose totale de 10 mg/kg
- AINS et l’aspirine : pas d’intérêt démontré, risque majoré d’ulcère gastro-duodénal de stress et de coagulopathie de consommation
- paracétamol : très peu efficace et risque d’aggravation de l’hépatite cytolytique
- A+B/Airway + Breathing :
- Adaptation du traitement en fonction des objectifs suivants :
- obtenir Température < 39 °C rapidement puis normalisation stable
- stabilisation hémodynamique : PAM 90 mmHg, FC 60 à 80 bpm, reprise de diurèse efficace
- disparition des troubles neurologiques
- traitement symptomatique des complications
- Température corporelle centrale (objectif < 39°C) et cutanée (objectif 30 à 33°C)/h
- Hémodynamique : PA, FC, FR, diurèse (après sondage urinaire)/h
- Neurologique : état de conscience (score de Glasgow), convulsions
- Autres : hémorragies, couleur des urines (rhabdomyolyse)
- Monitorage non invasif : scope, SpO2, glycémies capillaires, hémoglobine capillaire
- Monitorage invasif de la PA si état de choc non contrôlé par le remplissage initial
- Bilan biologique précédemment décrit / 4 à 6 h selon évolution
- Autres examens guidés par l’évolution clinique et biologique
- Dans tous les cas, hospitalisation pour traitement et surveillance
- Admission aux urgences en SAUV ou directement en réanimation
- Température corporelle stable < 37°5 C depuis plus de 24 h
- Hémodynamique normale et stable 24 h après arrêt du remplissage
- Bilan biologique normalisé : rhabdomyolyse, bilan rénal, ionogramme, bilan hépatique, hémostase
- Entraînement sportif régulier
- Efforts à la mesure des capacités physiques du patient
- Acclimatation avant l’effort si zone chaude et humide
- Protection solaire et thermique en cours d’effort (casquette, tee-shirt manches longues « respirant », brumisation régulière de la peau nue)
- Hydratation suffisante avant, pendant et après l’effort
- Arrêt immédiat de l’effort dès l’apparition des prodromes
- Prévenir ascendants, fratrie, descendants
- Biopsies musculaires, étude génétique
- Hyperthermie « exogène », par perte de capacité de thermorégulation au cours de l’effort avec :
- d’une part augmentation de la thermogénèse, liée à l’effort
- d’autre part réduction de la thermolyse : réduction des pertes thermiques cutanées (radiation, sudation – évaporation, convection, conduction) et respiratoires (air chaud saturé en eau)
- Hyperthermie « endogène » dans un second temps avec, fièvre liée aux mécanismes inflammatoires et secondairement au développement d’un véritable sepsis par translocation bactérienne à l’étage intestinal, puis cercle vicieux.
- Choc distributif en raison de la vasodilatation périphérique en réponse à la chaleur (mécanisme vaso-réflexe thalamique)
- Choc hypovolémique en raison de la sudation profuse secondaire à cette même vasodilatation périphérique
- Choc septique secondaire à la bactériémie provoquée par la translocation bactérienne, secondaire à la vasoconstriction splanchnique
- Insuffisance rénale aiguë fonctionnelle puis lésionnelle
- Insuffisance hépatocellulaire aiguë hémodynamique
- Risque de coagulopathie de consommation, avec choc hémorragique secondaire venant aggraver les mécanismes de choc pré existants
- Insuffisance coronarienne aiguë, etc.
- Décès dans un tableau de défaillance multiviscérale
- Algorithme coup de chaleur d’exercice
 _34
_34
Algorithme
Algorithme : coup de chaleur d’exercice Bibliographie- Bouchama A, Cafege A, Devol EB, Labdi O, el-Assil K, Seraj M. Ineffectiveness of dantrolene sodium in the treatment of heatstroke. Crit Care Med 1991;19:176-80.
- Bouchama A , Knochel JP . Heat stroke. N Engl J Med. <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>2002;346:1978-88.</javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>Bouchama A, Dehbi M, Chaves-Carballo E. Cooling and hemodynamic management in heatstroke: practical recommendations. Crit Care 2007;11:R54.</javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>Broessner G , Beer R , Franz G , Lackner P , Engelhardt K , Brenneis C , Pfausler B , Schmutzhard E . Case report: severe heat stroke with multiple organ dysfunction – a novel intravascular treatment approach. Crit Care <javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);>2005;9:R498-501.</javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);>Clements JM, Casa DJ, Knight J, McClung JM, Blake AS, Meenen PM, Gilmer AM, Caldwell KA. Ice-water immersion and cold-water immersion provide similar cooling rates in runners with exercise-induced hyperthermia. J Athl Train 2002;37:146-150.</javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);>Hadad E, Cohen-Sivan Y, Heled Y, Epstein Y. Clinical review: Treatment of heat stroke: should dantrolene be considered? Crit Care 2005;9:86-91.</javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);>Hadad E, Rav-Acha M, Heled Y, Epstein Y, Moran DS. Heat stroke : a review of cooling methods. Sports Med 2004;34:501-11.</javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);>Hausfater P. Dantrolene and heatstroke: a good molecule applied in an unsuitable situation. Crit Care 2005;9:23-4.</javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);>Hausfater P, Juillien G, Madonna-Py B, Haroche J, Bernard M, Riou B . Serum procalcitonin measurement as diagnostic and prognostic marker in febrile adult patients presenting to the emergency department. Crit Care 2007;11:R60.</javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);>Proulx CI , Ducharme MB , Kenny GP . Effect of water temperature on cooling efficiency during hyperthermia in humans. J Appl Physiol. <javascript:al_get(this,%20’jour’,%20’j%20appl%20physiol.’);>2003;94:1317-23.</javascript:al_get(this,%20’jour’,%20’j%20appl%20physiol.’);></javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);><javascript:al_get(this,%20’jour’,%20’j%20appl%20physiol.’);>Smith J, Wallis L. Cooling methods used in the treatment of exertional heat illness. Br J Sports Med 2005;39:503-7.</javascript:al_get(this,%20’jour’,%20’j%20appl%20physiol.’);></javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);><javascript:al_get(this,%20’jour’,%20’j%20appl%20physiol.’);>Sucholeiki R. Heatstroke. Semin Neurol 2005;25:307-14.</javascript:al_get(this,%20’jour’,%20’j%20appl%20physiol.’);></javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- <javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);><javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);><javascript:al_get(this,%20’jour’,%20’j%20appl%20physiol.’);>Varghese G, John G, Thomas K, Abraham O, Mathai D. Predictors of multi-organ dysfunction in heatstroke. Emerg Med J 2005;22:185-7.</javascript:al_get(this,%20’jour’,%20’j%20appl%20physiol.’);></javascript:al_get(this,%20�??’jour’,%20’crit%20care.’);></javascript:al_get(this,%20’jour’,%20’n%20engl%20j%20med.’);>
- Pour plus des conseils sur cette application et developpement de cette dernier contacter avec moi dans ma emaile support@mededuct.com

 _264
_264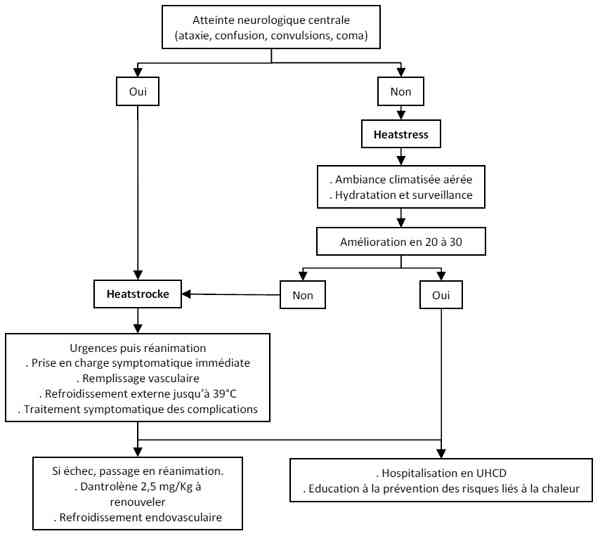 _34
_34